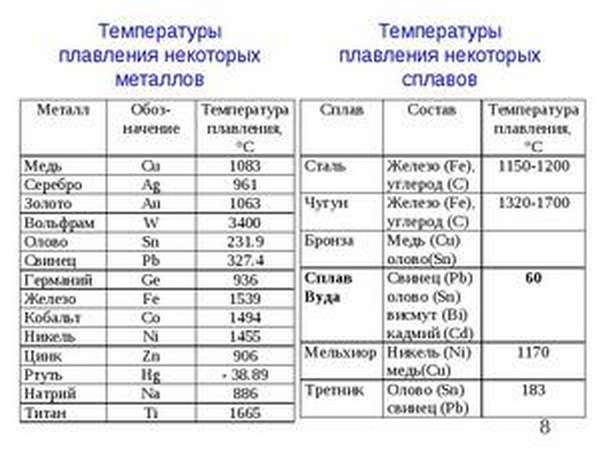
Свойства цинка, его температура и особенности плавления
Цинк или Zincum является 30 элементом периодической системы химических элементов Менделеева и обозначается символом Zn . В основном он используется при создании деформированных полуфабрикатов и в составе разного рода смесей. В чистом виде выглядит как хрупкий металл голубовато-серебристого цвета, быстро окисляется и покрывается защитной пленкой (оксидом), из-за которой заметно тускнеет.
Добывают его в Казахстане, Австралии, Иране и Боливии. Из-за сложностей в определении металла его часто называют «обманкой». Содержание
Историческая справкаСамо название «цинк» впервые было упомянуто в книге « Liber Mineralium » Парацельса. По некоторым данным оно означало «зубец». Сплав цинка с медью или латунь известен давно. Его применяли в Древней Греции, Индии и Древнем Египте, позднее материал стал известен в Китае.В чистом виде металл удалось получить лишь в первой половине XVIII века в 1738 году в Великобритании при помощи дистилляционного способа. Его открывателем стал Уильям Чемпион. Промышленное производство началось через 5 лет, а в 1746 году в Германии химик Андреас Сигизмунд Маргграф разработал и в деталях описал собственный способ получения цинка. Он предлагал использовать метод прокаливания смеси окиси металл с углем в огнеупорных ретортах из глины без доступа воздуха. Последующая конденсация паров должна была проходить в холодильнике. Из-за подробного описания и кропотливых разработок Маргграфа часто называют первооткрывателем вещества. В начале XIX века был найден способ выделения металла путем прокатки при 100 C о-150 C о. В начале следующего века научились добывать цинк электролитическим способом. В России первый металл получили только в 1905 году. Физические свойства
Цинк обладает слабыми механическими свойствами, при нормальной температуре легко ломается и крошится, но при температуре 100 C о-150 C о становится довольно тягучим и легко поддается деформации: куется, раскатывается в листы. Простая вода для металла безопасна, а кислоты и щелочи легко разъедают. Из-за этого цинк в чистом виде для изготовления деталей не применяют, только сплавы. Химические свойства Внешняя электронная конфигурация одного атома цинка можно записать как 3 d 104 s 2. Металл активен и является энергичным восстановителем. При температуре в 100 C она открытом воздухе покрывается пленкой, состоящей из основных карбонатов, и сильно тускнеет. При воздействии углекислого газа и повышенной влажности элемент начинает разрушаться. В кислородной или обычной среде при сильном нагревании цинк сгорает, образуя голубоватое пламя и белый дым, который состоит из оксида цинка. Огнеопасно воздействуют на цинк сухие элементы фтора, брома и хлора, но только при участии паров воды. Внешняя электронная конфигурация одного атома цинка можно записать как 3 d 104 s 2. Металл активен и является энергичным восстановителем. При температуре в 100 C она открытом воздухе покрывается пленкой, состоящей из основных карбонатов, и сильно тускнеет. При воздействии углекислого газа и повышенной влажности элемент начинает разрушаться. В кислородной или обычной среде при сильном нагревании цинк сгорает, образуя голубоватое пламя и белый дым, который состоит из оксида цинка. Огнеопасно воздействуют на цинк сухие элементы фтора, брома и хлора, но только при участии паров воды. При соединении металла и сильных минеральных кислот первый растворяется, особенно если смеси нагреть, в результате образуются соответствующие соли. Щелочи, расплавы и растворы окисляют вещество, в результате образуются цинкиты, растворимые в воде, и выделяется водород. Интенсивность воздействия кислот и щелочей зависит от наличия в цинке примесей. Чем более «чист» металл, тем слабее он взаимодействует из-за перенапряжения водорода. Содержание в природеКак самостоятельный элемент цинк в природе не встречается. Его можно добыть из 66 минералов, среди которых сфалерит, каламин, франклинит, цинкит, виллемит, смитсонит. Первый является наиболее распространенным источником металла, его часто называют «цинковой обманкой». Он состоит из сульфида цинка и примесей, которые придают минералу разнообразные цвета. Это осложняет его поиск и правильное определение. Найти цинк можно в кислых и изверженных породах — во последних его немного больше. Часто металл в виде сульфида вместе со свинцом встречается в термальных водах, мигрирует в поверхностных и подземных источниках. Особенности выплавки Температура, необходимая для плавления цинка, должна быть меньше 419 C о, но и не больше 480 C о. В противном случае вырастет угар металла и повысится износ стенок ванны, которую стандартно производят из железа. В расплавленном состоянии допускается не более 0,05% примеси железа, иначе температура, нужная при плавлении, начнет повышаться. Если процент содержания железа будет превышать 0,2%, цинк нельзя будет подвергать прокатке. Температура, необходимая для плавления цинка, должна быть меньше 419 C о, но и не больше 480 C о. В противном случае вырастет угар металла и повысится износ стенок ванны, которую стандартно производят из железа. В расплавленном состоянии допускается не более 0,05% примеси железа, иначе температура, нужная при плавлении, начнет повышаться. Если процент содержания железа будет превышать 0,2%, цинк нельзя будет подвергать прокатке. Цинк получают из полиметаллических руд, в которых может содержаться до 4% элемента. Если руды были обогащены селективной флотацией, из них можно получить до 60% цинковых концентратов, остальное будет занято концентратами других металлов. Цинковые концентраты обжигают в печах в кипящем слое, после чего сульфид цинка переходит в оксид, и выделяется сернистый газ. Последний идет в расход: из него получают серную кислоту. Чтобы перевести оксид цинка в сам металл, используют два способа. Смеси и сплавы Для усиления прочности и увеличения температуры плавления металл смешивают с медью, алюминием, оловом, магнием и свинцом. Для усиления прочности и увеличения температуры плавления металл смешивают с медью, алюминием, оловом, магнием и свинцом. Самым известным и востребованным сплавом является латунь. Это смесь меди с добавлением цинка, иногда встречаются и олово, никель, марганец, железо, свинец. Плотность латуни достигает 8700 кг/м3 . Температура, нужная для плавления, держится на отметке 880 C о — 950 C о: чем больше в ней содержание цинка, тем она ниже. Сплав отлично сопротивляется неблагоприятной внешней среде, хоть и чернеет на воздухе, если не покрыта лаком, прекрасно полируется и сваривается контактной сваркой. Существует два вида латуни: Сплав Zamak или Zamac состоит из цинка, алюминия, меди и магния. Само название образовано из первых букв латинских названий: Zink — Aluminium — Magnesium — Kupfer / Cuprum (Цинк-Алюминий-Магний-Медь). В СССР сплав был известен как ЦАМ: Цинк-Алюминий-Медь. Активно применяется в литье под давлением, плавление начинается при низкой температуре (381 C о — 387 C о) и имеет низкий коэффициент трения (0,07). Обладает повышенной прочностью, что позволяет получать изделия сложной формы, которые не боятся сломаться: дверные ручки, клюшки для гольфа, затворы огнестрельного оружия, строительную фурнитуру, застежки разных видов и рыболовные снасти. Небольшой процент цинка (не более 0,01%) содержится в гартовых сплавах, применяемых в полиграфии для отливки типографских шрифтов и линеек, печатных форм и машинного набора. Это устаревшие смеси, на место которых пришел чистый цинк с небольшим добавлением примесей. Невысокая температура, которая требуется для плавления цинка, часто компенсируется за счет сплавов с другими металлами, но бывает и наоборот. Если температура, необходимая для плавления «чистого» металла, составляет 419,5 C о , то сплав с оловом снижается до 199 C о, а с оловом и свинцом — до 150 C о. И хотя такие сплавы можно паять и варить, чаще всего смеси с цинком применяют только для заделки имеющихся дефектов из-за их слабой прочности. Например, сплав олова, свинца и цинка рекомендуется применять только на никелированных изделиях. Чаще всего цинковые сплавы применяют для создания карбюраторов, рам спидометров, радиаторных решеток, гидравлических тормозов, насосов и декоративных элементов, деталей для стиральных машин, миксеров и кухонного оборудования, часовых корпусов, пишущих машинок, кассовых аппаратов и бытовой техники. Эти детали нельзя применять в промышленном производстве: при повышении температуры до 100 C о прочность изделия снижается на треть, а твердость — почти на 40%. При понижении температуры до 0 C о цинк становится слишком хрупким, что может привести к поломке. ПрименениеЦинк является одним из наиболее востребованных металлов в мире: он находится на третьем месте по объему добычи среди цветных металлов, уступая только меди и алюминию. Этому способствует и его невысокая цена. Чаще всего его применяют для защиты от коррозии и в качестве части сплава, например, латуни.  В металлургии цинк особенно ценен. Его наносят тонким слоем на стальную поверхность многих металлоконструкций, чтобы полностью защитить их от ржавчины на механическом и химическом уровне. На это расходуется до 40% от всей добычи. Поскольку цинк, в отличие от никеля, кобальта, олова и кадмия, активнее железа, он первым начинает контактировать с недружелюбной внешней средой, полностью защищая основу. В металлургии цинк особенно ценен. Его наносят тонким слоем на стальную поверхность многих металлоконструкций, чтобы полностью защитить их от ржавчины на механическом и химическом уровне. На это расходуется до 40% от всей добычи. Поскольку цинк, в отличие от никеля, кобальта, олова и кадмия, активнее железа, он первым начинает контактировать с недружелюбной внешней средой, полностью защищая основу.В живых организмахВ теле человека содержится около 2 граммов цинка, около 400 ферментов содержат его. К последним относятся ферменты, катализирующие гидролиз белков, сложных эфиров и лептидов, полимеризацию РНК и ДНК, образование альдегидов. Чистый элемент содержится в мышцах, поджелудочной железе и печени. В день мужчинам требуется 11 мг цинка, женщинам — 8 мг. В организме цинк выполняет следующие функции:  Нормализует деятельность простаты; Нормализует деятельность простаты;При недостатке элемента в организме наблюдается быстрая утомляемость, раздражительность, потеря памяти, снижение зрения и веса без объективной причины, приступы аллергии, депрессивное состояние. Происходит понижение уровня инсулина и накопление в теле некоторых элементов: железа, свинца, меди, кадмия. В продуктах питанияЭлемент имеется в мясе, сыре, кунжуте, устрицах, шоколаде, бобовых, овсянке, подсолнечных и тыквенных семечках, часто присутствует в минеральной воде. Наибольший процент цинка содержится в следующих продуктах (из расчета на 100 грамм): Опасность для человекаОтравление цинком обычно происходит при длительном вдыхании его паров. Первыми признаками являются сильная жажда, потеря аппетита, сладковатый привкус во рту. Нередко появляется усталость, сонливость, сухой кашель, чувство разбитости, давящая боль в грудной клетке. Длительное воздействие может привести к бесплодию, малокровию, задержке в развитие. В быту опасность представляет оцинкованная посуда, в которой длительно хранится пища.
|
Загрузка. Пожалуйста, подождите...